栄養
Nutrition
あなたは、あなたが食べてきたそのものです
Nutrition
あなたは、あなたが食べてきたそのものです
2023.04.28
今回も前回の投稿に引き続き「タンパク質の過剰摂取」についてのお話しです。
近年の栄養学の神話の一つと言われているのが、「栄養はたくさん摂れば摂るほど良い」というものです。
およそ5500万年前に最初の原始霊長類が出現したと考えられていますが、人類の歴史がどのようなものであったとしても、わたしたちの祖先が、今日のように「最小限に運動して」「最大限に食べる」といったライフスタイルは、どの時代においてもありませんでした。
しかし、想像を絶する過酷な生活環境にあったにもかかわらず、今日、世界中に蔓延している「生活習慣病・慢性病」という疾病も無かったのです。
現代の病気は、「食べ過ぎ=過剰栄養」と「エンプティ・カロリー食」による「栄養失調」、そして「有害な食品」の過剰摂取など、「食源病」によるものが大半を占めています。
※ エンプティ・カロリー:カロリーは高いのに、栄養は空っぽ。つまり「肥満」と「現代の栄養失調」の両方を引き起こす、ジャンクフード(超加工食品)のことです。
3大栄養素の中でも、過剰摂取による悪害が最も大きいと考えられているのが「タンパク質」なのです。
さらに、タンパク質(動物性)ともっとも相性が悪いのが、「便秘」です。
つまり、動物性タンパク質の過剰摂取、未消化のタンパク質を腸内細菌(マイクロバイオーム)が分解 =腸内異常発酵(腐敗)、有害な腐敗産物の発生、血流に載った有害物質の全身循環、老化の進行、体臭・口臭の悪化、病気の発症という負のサイクルです。
油断は大敵、気をつけたいですね!
では、つづきをご覧ください。

Digestive Disorder. Woman Suffering From Constipation Sitting On Toilet In Restroom Indoors. Defecation Problem And Hemorrhoids Concept.
多くの研究データにより、高タンパク質食の摂取は、ヒトの健康にとって好ましいものではなく、糖尿病や心血管系疾患の発症リスクの増大と関係することが示されています。[26-30]
2型糖尿病の発症リスクは、1日のタンパク質摂取量が64gを超えて10g増えるごとに20-40%増加すると推定されています。[31-33]
一方、タンパク質の摂取量を減らすことは、代謝系機能に対して有益な効果をもたらすことが報告されています。[34]

Comparison of female face after incredible rejuvenation process or heavy retouching
ルイージ・フォンタナ博士らの研究グループが、ウィスコンシン大学(University of Wisconsin)のダドリー・ラミング(Dudley Lamming)教授と行なった共同研究において、タンパク質の摂取量を適度に減らすことで(沖縄の百寿者の摂取量に近い値にすることで)、代謝機能が改善することがマウスとヒトの両方で確認されています。
エネルギー量が同じ食事でも、タンパク質のエネルギー比が7-9%の食事を摂取した人では、わずか4週間のうちに体重が2.6kg減少し、空腹時血糖も有意に低下していたと報告されています。[35]
さらに、低タンパク質食を摂取した被験者では、寿命延伸効果を有するホルモンといわれているFGF21の血中濃度が倍増していたといいます。[36]
併行して行なわれた動物実験では、タンパク質のエネルギー比が21%の標準的な飼料を2ヵ月間にわたって与えられたマウスに比べて、タンパク質のエネルギー比が7%の飼料を与えられたマウスでは、体重増加が少ないという結果が得られています。[37]
このとき、低タンパク質食を摂取したマウスでは、飼料の摂取量はむしろ多くなっていたにもかかわらず、このような効果が得られていたのです。
ミッテンドーファー(Mittendorfer)教授による臨床研究において、通常のタンパク質食(0.8 g/kg体重)ではなく、高タンパク質食(1.3g/kg体重)を摂取した肥満者では、体重を10%減らした場合に通常であればみられるはずのインスリン感受性の改善効果(減量による主な目的の1つ)が、得られなくなることが報告されています。[38]
つまり、高タンパク質食を摂取した肥満女性では、体重が10%減少した(内臓脂肪や肝臓の脂肪も顕著に減少した)にもかかわらず、依然としてインスリン抵抗性を有し、2型糖尿病の発症リスクが高いままであることを意味しているわけです。
インスリン抵抗性とそれにともなう高インスリン血症は、インスリン/IGF-1経路を活性化し、老化およびガンの発症を促進することが分かっているのです。

Conceptual fat overweight obese female vs slim fit healthy body after weight loss or diet with muscles thin young woman over sunset. 3D illustration
いくつかの疫学研究では、高タンパク質食の摂取により、全死亡率が増大するという可能性が示唆されています。
たとえば、6,381名の成人を対象として行なわれたアメリカ国民健康・栄養調査(National Health and Nutrition Examination Survey: NHANES)において、高タンパク質食を摂取している50-65歳の男女では、18年間の追跡調査期間中における全死亡率が75%高く、さらにガンおよび糖尿病による死亡率も4倍高かったことが明らかとなっています。[39]
動物実験においても、このことを支持する結果が得られています。
三大栄養素の中で過剰摂取が、老化や死亡率にもっとも大きな影響を及ぼすものはタンパク質だと考えられています。
多くの動物種において、最長寿命を記録したのは、低タンパク質・高炭水化物食を摂取した場合であり、タンパク質と炭水化物の最適な比率は1: 10で、タンパク質のエネルギー比率は全体の10%程度にまで低くしたほうがよいといわれているのです。[40]
マウスでは、食餌中の炭水化物(糖質)に対するタンパク質の比率を減らすにしたがって、平均寿命が~30%ほど延びることが報告されています。[41]
興味深いことに、世界でもっとも寿命の長い地域である日本の沖縄の伝統的な食事では、タンパク質からのエネルギー摂取量が全体のわずか9%程度になっています。
以上のような動物実験やヒト試験で得られた結果は、以下の2つの誤った考え方を覆す非常に重要なものでと言えるでしょう。
1.エネルギーはエネルギー以上の意味をもたない。
2.高タンパク質食は健康によいものであり、肥満を予防したり、筋量を増やしたり、さらには健康的に長生きするうえで重要なものである。
日常的にタンパク質、特に動物性のタンパク質(分岐鎖アミノ酸および含硫アミノ酸を豊富に含むタンパク質)を多量に摂取することは控えなければなりません。
なぜなら、高タンパク質食の摂取は、体脂肪量の増加や糖尿病、心血管系疾患およびガンの発症さらには早期死亡のリスクを増大させるからなのです。
そして忘れてはならないのは、「高タンパク質食 × 便秘 = 腸内異常醗酵 = 有害物質による疾病リスクの増大」という問題です。
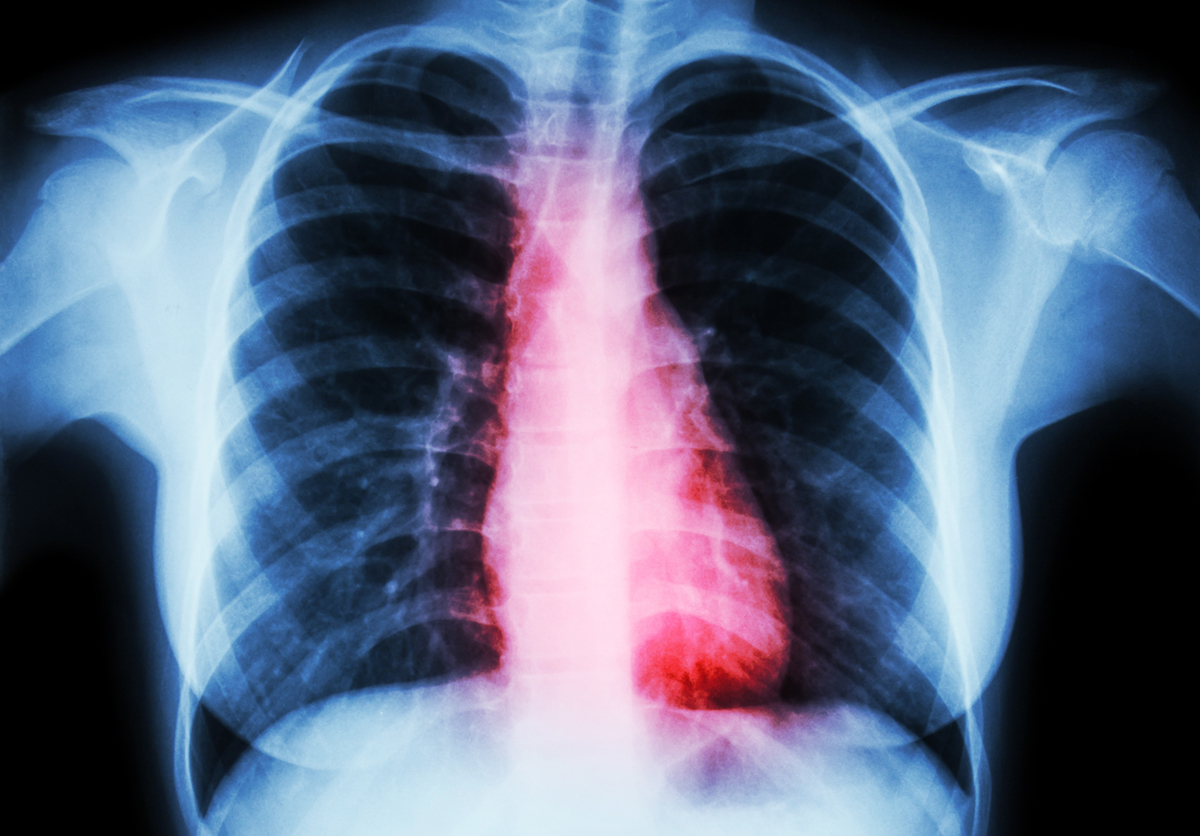
Heart disease ( Film chest x-ray of woman with heart disease )
タンパク質には数えきれないほど多くの種類のものがあり、長く、入り組んだペプチド鎖によって構成されています。
さらに、タンパク質(ペプチド)の最小構成単位はアミノ酸で、そのアミノ酸には20種類のものがあります。
20種類のアミノ酸のうち、9つ(ロイシン、イソロイシン、メチオニン、フェニルアラニン、バリン、スレオニン、 トリプトファン、リジン、ヒスチジン)は、体内で合成することができず、食事から摂取しなければならないため、「必須アミノ酸(不可欠アミノ酸)」と呼ばれています。

Animal protein
肉類、卵、チーズには、必須アミノ酸がすべて含まれています。
しかしながら、そのような動物性食品を摂取した場合、以下のものも同時に摂取することになります。
・過剰量の飽和脂肪酸(それにより、高コレステロール血症につながる)[42]
・コリン、Lーカルニチン(腸内細菌による発酵および肝臓での代謝を経て、トリメチルアミンNーオキシド(trimethylamine N-oxide: TMAO)に代謝される。TMAOは、冠動脈におけるアテローム性プラークの形成を促進する)[43]
・過剰量の鉄(酸化ストレスを惹起し、結腸ガンの発症リスクを高める)[44]
・高容量のメチオニンおよび分岐鎖アミノ酸(IGF/mTOR経路を活性化することで、インスリン抵抗性、2型糖尿病、ガンの発症リスクを高め、老化を促進する)[45]
ランダム化比較試験では、高タンパク質食(乳製品や肉類およびホエイプロテインサプリメントなどによって構成される食事)の摂取は、インスリン感受性を大きく低下させ、血中インスリン濃度を上昇させるという一致した結果が報告されています─つまり、糖尿病のリスクを高める。[46・47]
2型糖尿病患者を対象として行なわれた試験では、減量を目的とした2ヵ月間にわたる介入によって得られるはずであった糖代謝およびインスリン感受性の改善効果が、鶏肉、魚、卵、低脂肪乳およびチーズの多量摂取により認められなくなったという結果が報告されています。[48]
疫学研究において、タンパク質の総摂取量と2型糖尿病の発症率とのあいだに関係が認められています。
ただし、それは主に動物性タンパク質の摂取量によるものであるのに対して、植物性タンパク質の摂取量と2型糖尿病の発症率とのあいだにはむしろ負の相関関係が認められることが示されているのです。
この疫学研究の知見を支持しています。[49・50]

Woman making skin fold on stomach and injecting medicine from syringe at home. Continuous administration of insulin in treatment of type 2 diabetes mellitus concept
すべての必須アミノ酸と非必須アミノ酸が適切かつ完璧な組成で含まれているのは動物性食品だけであり、毎日、適切な量の動物性タンパク質を摂取しないと筋量や筋機能を保持・向上することはできない、という考え方は正しいのでしょうか?
シャイヤー・ホースと呼ばれる労働馬やホルスタイン(乳牛)のとても大きな筋肉をみたことがあるでしょうか?
彼らは典型的な草食動物で、主に牧草や干草を食ベオーツ麦(えん麦)のような全粒穀物をときどき摂取しています。
通常、成馬では、タンパク質は餌の中にわすか8-10%程度含まれていれば十分であるといわれています。

Shire Horse
同じことが、アフリカゾウ(体重が10.4トン程度にまで成長する陸上で最大・最重量の生物)や大人の雄ゴリラ(体重約260kg)にもいえます。
これは、植物性食品にも(その組成は植物によって異なるものの)必須アミノ酸が含まれているためなのです。
たとえば、豆類には、リジンが多く含まれていますが、トリプトファンやメチオニンの含有量はわずかです。
一方、全粒穀物には、リジンが少なく、トリプトファンやメチオニンが多く含まれています。
玄米とヒラ豆で構成される食事やヒヨコ豆と全粒粉パスタからなる食事であれば、完璧な組成のタンパク質─卵や肉類に含まれるタンパク質─と何ら変わりのないタンパク質を摂取できることになります。
1日の中で全粒穀物と豆類を組み合わせて摂取することが重要だといわれているのは、このような理由からなのです。
植物性タンパク質が代謝系機能に及ぼす効果が、動物性タンパク質によるものとなぜ異なるのか、ということはいまだ明らかとなってはいません。
おそらく、その一部は、アミノ酸組成の違いによるものではないかと考えられています。
近年の研究において、マウスに対して分岐鎖アミノ酸(乳製品、肉類、魚および卵に多く含まれるアミノ酸)の少ない餌を与えただけで、体重(体脂肪量)が減少し、血糖値も低下することが明らかとなっています。[51]
食事に含まれる分岐鎖アミノ酸は、インスリン抵抗性やガンの発症に関わっていることが示されており、さらに、ヒトにおいては、分岐鎖アミノ酸を代謝する酵素の発現量がガンによる死亡リスクの予測因子にもなっています。[52・53]
このような研究結果と同様に、他の研究においても、動物性タンパク質を植物性タンパク質に置き換えることで、異種移植モデルマウスにおける前立腺ガンおよび乳ガンの増殖が明確に抑制されたことが報告されています。[54]
この異種移植モデルとは、ヒト由来のガン細胞を免疫不全マウス(ヒトの細胞に対する拒絶反応を示さないマウス)へ移植する実験モデルのことです。
植物性タンパク質による2塑糖尿病やガンに対する予防効果は、植物性タンパク質に結合している有用な生理活性物質を多く摂取することによるものだという可能性もあります。

Diet change healthy lifestyle concept and having the courage to accept the challenge of losing weight as an overweight person on a high wire asparagus from fatty food towards vegetables and fruit.
また、疫学研究で得られたデータにおいても、動物性タンパク質を植物性タンパク質に置き換えることで、死亡率が低下する可能性が示されています。[55]
また、ハーバード大学医師・看護師健康調査(Harvard’s Physician and Nurse Health Studies)の参加者における全死亡リスクが、加工肉製品のタンパク質(エネルギー比:3%)を同じエネルギー量の植物性タンパク質で置き換えた場合に 34%低下すること、同様に、未加工の肉製品や卵製品のタンパク質を同じエネルギー量の植物性タンパク質で置き換えた場合にも、それぞれ12、19%低下することが明らかとなっています。[56]
このような疫学研究の結果は、肉類や乳製品に豊富に含まれるアミノ酸であるメチオニンの摂取量を制限することで平均寿命ならびに最長寿命が延びたという動物実験の結果と一致します。[57]
メチオニンの摂取量を、一般的な摂取量の65-80%程度に制限することで、ラットおよびマウスの寿命が30%延び、血糖値、IGF-1およびインスリン濃度も低下することが報告されています。[58]
植物性タンパク質に含まれるメチオニン量は少なく、このことも植物性タンパク質による健康効果ならびに抗老化効果(主に植物性食品を摂取している集団において認められている)に一部寄与していると考えられています。

Healthy Green food Clean eating selection Protein source for vegetarians: brussels sprouts, broccoli, spinach, spirulina, green peas on gray concrete background.
もともと欧米人は、肉食を主とする習俗民族ですが、永年にわたる経験から、心ある人は肉食にともなう有害性を身をもって体験したことから、あえて菜食主義を称えだしたのです。
古代ギリシャにおいてはピタゴラス、プラトン、アポロニオらは、その主導者でした。
中世紀になると、グレゴリオスや聖アウグスティヌス等の教父たちは、『旧約聖書』の創世記の、
神言ひたまひけるは、視よ我全地の面にある実蓏(み)のなる諸(すべて)の草蔬(くさ)と木果(くだもの)の結(な)る諸(すべて)の樹とを、汝等に与ふ。
これは汝らの糧となるべし。
の一節を揚言して、菜食主義を信徒に唱導していました。
近世紀に入ると、ジャン=ジャック・ルソー(Jean-Jacques Rousseau)、フリードリヒ・フォン・シラー(Johann Christoph Friedrich von Schiller)、アイザック・ニュートン(Sir Isaac Newton)、ベンジャミン・フランクリン(Benjamin Franklin)、トルストイ(Lev Nikolayevich Tolstoy)、エジソン(Thomas Alva Edison)等の傑人たちが、菜食主義を主張したことはあまりにも有名です。

Sir Isaac Newton
このような欧米の流れが、ついに1848年には英国マンチェスターに「菜食主義協会」となって結成され、また1868年にはドイツに「自然生活友の会」となって結実しました。
その後、フランス、アメリカ、オーストリア、デンマーク、イタリア、ロシアにもつぎつぎに菜食主義協会の設立がみられ、会員のための宿泊施設や料理店が開業されたのです。
中国においても、はやくから肉食の害を認め、『聞見録』に「人若し菜根を咬得(こうとく)すれば、すなわち百事なすべし」とあり、また朱文公の『倹徳帖』、司馬君実の『訓倹文』、孫真人の『枕上記』等にも菜食を賛した文句が見られます。
ちなみに、ベジタリアン(Vegetarian)は、1840年、英国ベジタリアン協会の前進「Alcott House」が出版した書物の中で、初めて登場した造語とみられています。
いかがでしたか?
長い間「最も良質なタンパク質は、動物性のタンパク質」だと信じられてきたました。
そして今日でもなお、この19世紀の間違った栄養学の亡霊は、わたしたちの食習慣に幅広くはびこっています。
驚くほど多くの人の頭の中にある栄養学は、19世紀のままなのです。
人体にとってタンパク質は重要な栄養素であるものの、「動物性の食品」を摂るか、「植物性の食品」を摂取するかで、健康に対する影響が大きく変わってきます。
動物性タンパク質の過剰摂取の有害性と植物性タンパク質の有効性は、西医学健康法の創始者・西勝造をはじめ、多くの臨床において生菜食の健康効果を立証した断食博士・甲田光雄などの知見とも一致します。
そして今日、さまざまな医学会のコンセンサス(一致した意見)でもあります。[59]
ハーバード大学のダニエル・リバーマン教授(古人類学者・ハーバード大学骨格生物学研究所の所長)は、生活習慣病を「ミスマッチ病」つまり、怠惰で不摂生な現代のライフスタイルがもたらす病気と呼び、率直にこう忠告しています。
あなたが死ぬときは、十中八九ミスマッチ病が原因だろう。
そしてさらに、
人々を死なせている病気の70パーセントは、もう少し分別のある生き方をするだけで簡単に予防できる。
そもそも、下記の原則を遵守する限り肥満になったり、心身に不調をきたすことはありません。
Eat real food.
(本物の食べ物を食べましょう)
Mostly plants.
(主に植物性食品)
Not too much.
(多すぎない程度に)
&
Smooth defecation.
(スムーズな排泄)
References
26.Malik. V. S., et al. Dietary protein intake and risk of type 2 diabetes in US men and women American journal of Epidemiology, 183. 715-728 (2016).
27.Shang. X., et al. Dietary protein intake and risk of type 2 diabetes: results from the Melbourne Collaborative Cohort Study and a meta-analysis of prospective studies. The American Journal of Clinical Nutrition. 104. 1352-1365 (2016)
28.Wang. E. T., de Koning. L. & Kanaya. A. M Higher protein intake is associated with diabetes risk in South Asian Indians: the Metabolic Syndrome and Atherosclerosis in South Asians Living in America (MASALA) study. The Journal of American College of Nutrition. 29, 130-135 (2010).
29.Simila. M. E., et al. Carbohydrate substitution for fat or protein and risk of type 2 diabetes in male smokers. European Journal of Clinical Nutrition. 66. 716-721 (2012)
30.Lagiou. P., et al. Low carbohydrate-high protein diet and mortality in a cohort of Swedish women. Journal of Internal Medicine, 261. 366-374 (2007).
31.Wang. E.T. Higher protein intake is associated with diabetes risk. The Journal of American College of Nutrition (2010).
32.Tinker. L. F., et al. Biomarker-calibrated dietary energy and protein intake associations with diabetes risk among postmenopausal women from the Women’s Health Initiative. The American Journal of Clinical Nutrition, 94. 1600-1606 (2011)
33.Sluijs. I., et al. Dietary intake of total. animal. and vegetable protein and risk of type 2 diabetes in the European Prospective Investigation into Cancer and Nutrition (EPIC) -NL study. Diabetes Care, 33. 43-48 (20l O).
34.Rand. W. M., Pellett. P. L. & Young. V. R. Meta-analysis of nitrogen balance studies. The American Journal of Clinical Nutrition (2003)
35.Fontana. L., et al. Decreased consumption of branched-chain amino acids improves metabolic health. Cell Reports. 16. 520-530 (2016)
36.Zhang. Y., et al. The starvation hormone, fibroblast growth factor-21. extends lifespan in mice, eLife, l. e00065 (2012)
37.Fontana. L., et al. Decreased consumption of branched-chain amino acids. Cell Reports (2016)
38.Smith. G. I., et al. High-protein intake during weight loss therapy eliminates the weight-loss-induced improvement in insulin action in obese postmenopausal women. Cell Reports. 17. 849-861 (2016).
39.Levine. M. E., et al. Low protein intake is associated with a major reduction in IGF-1, cancer. and overall mortality in the 65 and younger but not older population. Cell Metabolism. 19. 407-417 (2014).
40.Simpson. S. J., et al. Dietary protein. aging and nutritional geometry. Aging Research Reviews. 39. 78-86 (2017).
41.Solon-Biel. S. M., et al. The ratio of macronutrients. not caloric intake. Cell Metabolism (2014)
42.Mensink. R. Effects of saturated fatty acids on serum lipids and lipoproteins: a systematic re view and regression analysis. World Health Organization (2016).
43.Tang. W. H., et al. Intestinal microbial metabolism of phosphatidylcholine and cardiovascular risk. The New England Journal of Medicine. 368. 1575-1584 (2013).
44.Bastide. N. M., Pierre. F. H. & Corpet. D. E. Heme iron from meat and risk of colorectal cancer: a meta-analysis and a review of the mechanisms involved. Cancer Prevention Research. 4. 177-184 (2011).
45.Efeyan. A., Zoncu. R. & Sabatini. D. M. Amino acids and mTORCl: from lysosomes to disease Trends in Molecular Medicine. 18. 524-533(2012)
46.Weickert. M. O., et al. Effects of supplemented isoenergetic diets differing in cereal fiber and protein content on insulin sensitivity in overweight humans. The American journal of Clinical Nutrition. 94. 459-471 (2011).
47.Hattersley. J. G., et al. Modulation of amino acid metabolic signatures by supplemented isoenergetic diets differing in protein and cereal fiber content. The Journal of Clinical Endocrinology and Metabolism. 99. £25992609 (2014)
48.Sargrad. K. R., et al. Effect of high protein vs high carbohydrate intake on insulin sens1t1v1ty. body weight. hemoglobin Ale. and blood pressure in patients with type 2 diabetes mellitus Journal of the American Dietetic Association. 105.573-580 (2005).
49.Malik, V. S., et al. Dietary protein intake. American Journal of Epidemiology (2016)
50.Sluijs. I., et al. Dietary intake of total. animal. and vegetable protein and risk of type 2 diabetes. Diabetes Care (2010)
51.Fontana. L., et al. Decreased consumption of branched-chain amino acids. Cell Reports (2016)
52.Smith. G. I., et al. Protein ingestion induces muscle insulin resistance independent of leucine-mediated mTOR activation. Diabetes. 64. 1555-1563 (2015).
53.Ericksen, R. E., et al. Loss of BCAA catabolism during carcinogenesis enhances mTORC1 activity and promotes tumor development and progression. Cell Metabolism. 29. 1151-1165. ell56 (2019)
54.Fontana, L., et al. Dietary protein restriction inhibits tumor growth in human xenograft models of prostate and breast cancer. Oncotarget. 4. 2451 (2013)
55.Levine. M. E., et al. Low protein intake 1s associated with a major reduction in IGF-1. cancer. Cell Metabolism (2014)
56.Song, M., et al. Association of animal and plant protein intake with all-cause and cause-specific mortality. Journal of the American Medical Association: Internal Medicine, 176. 1453-1463 (2016)
57.Ables. G. P., et al. The first international mini-symposium on methionine restriction and lifespan. Frontiers in Genetics. 5. 122 (2014)
58.Miller. R. A., et al. Methionine-deficient diet extends mouse lifespan. slows immune and lens aging, alters glucose. T4. IGF-I and insulin levels. and increases hepatocyte MIF levels and stress resistance. Aging Cell. 4. 119-125 (2005).
59.Kayli Anderson, et al. Popular fad diets: An evidence-based perspective. Progress in cardiovascular diseases. 2023 Mar 03; pii: S0033-0620(23)00007-5.
This article has been edited based on the summary of “The Path to Longevity – The Secrets to Living a Long, Happy, Healthy Life” by Luigi Fontana.
 トップへ戻る
トップへ戻る